Физика - Поурочные разработки 11 класс - 2017 год
Испускание и поглощение света атомами. Спектры - АТОМНАЯ ФИЗИКА - КВАНТОВАЯ ФИЗИКА
Задачи урока: познакомить с линейчатыми спектрами, способами их получения, механизмами возбуждения атомов, со спектрами поглощения; изучить линейчатый спектр (ДЭ-2, с. 217—219); продолжить формирование умений выделять и описывать физические явления.
План урока
|
Этапы урока |
Время, мин |
Приёмы и методы |
|
I. Повторение |
8—10 |
Решение задач. Ответы на вопросы |
|
II. Изучение нового материала |
12—15 |
Рассказ учителя. Опыты. Беседа. Записи в тетрадях. Рисунки |
|
III. Самостоятельная работа |
20 |
Решение задач. Работа с учебником |
|
IV. Домашнее задание |
1—2 |
Запись на доске |
I. Вновь повторяют постулаты Бора, формулу для энергии электрона в атоме водорода, энергетическую диаграмму. У доски во время фронтального опроса решают и обсуждают задачу.
II. Изучение нового материала начинается с обсуждения вопроса: что происходит при переходе атома из одного стационарного состояния в другое? Он составляет основу учебной проблемы урока.
Беседа продолжается по вопросам: можно ли с помощью постулатов Бора и формулы Планка определить частоту излучаемых (поглощаемых) электромагнитных волн? Что нужно знать, чтобы рассчитать эту частоту для атома водорода?
Подставляя значения энергии
![]()
в известную формулу
![]()
получаем при переходе из состояния k в состояние n следующее выражение для частоты излучения:
![]()
где k, n = 1, 2, 3, ...; k > n.
Если переход происходит из более высокого энергетического состояния в более низкое, то энергия излучается, а если наоборот — поглощается. Из выведенной формулы видно, что атом водорода может излучать и поглощать электромагнитные волны не любых, а определённых частот.
Совокупность входящих в излучение волн определённых частот называется спектром. Спектр изучают с помощью спектроскопов с призмой или дифракционной решётки. Спектр солнечного света состоит из почти непрерывной совокупности волн с различными длинами волн (рассматривают рисунок в учебнике). Спектр же атома водорода или какого-либо другого атома состоит из волн определённых длин волн, на экране получается совокупность отдельных узких линий. Спектр излучения и поглощения атома линейчатый. (Рассматривают линейчатые спектры на цветной вклейке учебника.)
Учитель может сообщить, что учёные изучали спектры задолго до выяснения строения атома. Длины волн (а значит, и частоты) излучения измерялись с высокой степенью точности. Экспериментально была получена, в частности, формула для частот излучения водорода:
![]()
где R — постоянная, названная в честь шведского спектроскописта Ридберга. Она измерена опытным путём: ![]() Ранее мы получили аналогичную формулу теоретически. Осталось сравнить экспериментальное значение константы R с теоретически рассчитанным:
Ранее мы получили аналогичную формулу теоретически. Осталось сравнить экспериментальное значение константы R с теоретически рассчитанным:
![]()
Таким образом, экспериментальное значение константы согласуется с теорией атома водорода по Бору, что подтверждает правильность постулатов последней.
Рассмотрим энергетический баланс излучения. Для того чтобы атом излучал, необходимо его возбуждение, т. е. сообщение энергии извне, так как в обычном — основном невозбуждённом — состоянии атомы имеют наименьшее значение энергии. Существуют различные механизмы возбуждения атомов.
На практике используют оптическое возбуждение: под действием света (электромагнитных волн) атом приобретает энергию и переходит из низших энергетических состояний в высшие. При этом в соответствии с дискретным характером уровней атом может поглотить не любой квант, а только такой, энергия которого равна разности энергий двух уровней атома. Последнее означает, что атомы поглощают электромагнитные волны той же частоты, что и излучают.
Пусть мы имеем свет всевозможных частот. Если его пропустить через газ, состоящий из атомов (можно показать на опыте), то на экране на фоне сплошного спектра появятся тёмные линии поглощения. Это линейчатый спектр поглощения.
Существуют и другие способы возбуждения атомов, например тепловой. Если тело (в твёрдом, жидком, газообразном состоянии) нагревать, то хаотичное движение атомов ускоряется, при соударениях атомы получают энергию, необходимую для возбуждения. В результате вещество начинает испускать свет.
В заключение надо остановиться на вопросе о причинах перехода атома из высшего энергетического состояния в низшее. Согласно первому постулату Бора атом в стационарном состоянии не излучает и не поглощает, т. е. сам по себе из одного состояния в другое не переходит. Второй постулат говорит только об излучении при переходе, но не говорит о причине перехода.
Различают два вида излучения: вынужденное (индуцированное) и самопроизвольное (спонтанное). В первом случае причиной перехода атома из более высокого энергетического состояния в более низкое является внешнее воздействие на атом. Такое воздействие оказывает, в частности, электромагнитная волна или свет подходящей частоты. Но даже при отсутствии внешних воздействий атом через миллиардные доли секунды переходит из возбуждённого состояния в основное. Это — спонтанное излучение. Конечно, процесс спонтанного излучения протекает в соответствии с законом сохранения энергии, но он противоречит постулату Бора о стационарных состояниях. Однако в квантовой механике выясняется, что внешнее воздействие на атом есть и в этом случае: на микроуровне электромагнитное поле в вакууме всегда имеет место, даже если макроскопическая электромагнитная волна отсутствует. Это поле и вызывает спонтанные переходы.
III. Последний этап урока проходит в форме самостоятельной работы по выполнению упражнений. Используется учебник, записи в тетрадях. Учитель консультирует отдельных учеников.
Приводим примеры заданий, которые могут быть даны по вариантам.
1. Определите энергию фотонов, соответствующих излучению атома водорода в видимой части спектра (см., например, рисунок V на цветной вклейке учебника).
2. С помощью формулы энергии постройте диаграмму энергетических уровней атома водорода (пять-шесть состояний). Постоянно ли расстояние между уровнями? При каких значениях nрасстояние между ними меньше? Какую наименьшую и наибольшую энергии может излучить атом при переходе между уровнями? Может ли атом водорода излучить (поглотить) квант энергии 9,0 эВ? Можем ли мы увидеть излучение атома водорода, возникшее в результате перехода с четвёртого энергетического уровня на первый? Есть ли это излучение в спектре водорода на цветной вклейке?
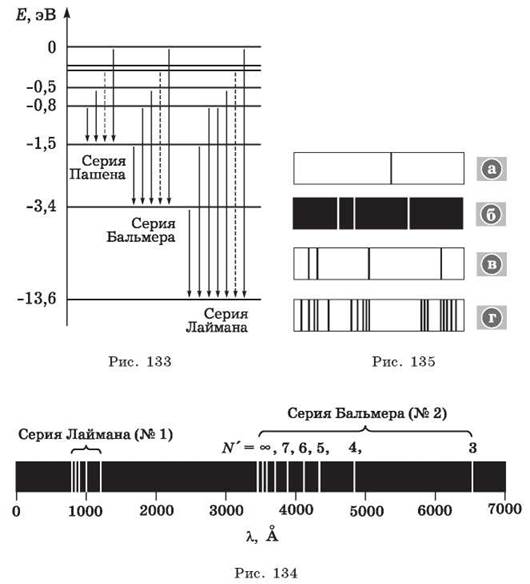
3. Пользуясь диаграммой энергетических переходов атома водорода (рис. 133, 134), объясните, которая из серий переходов даёт инфракрасное, ультрафиолетовое, видимое излучения.
4. Какой из приведённых на рисунке 135 спектров является спектром излучения атома водорода?
IV. Домашнее задание: § 67*, 75, 77* (3, 4); упр. на с. 298 (5); индивидуально - П., № 828.